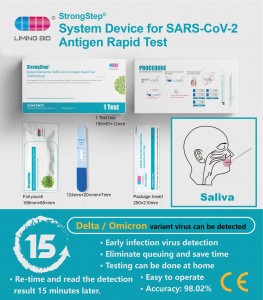
Proba rápida do antíxeno SARS-CoV-2 (nasal)
O produto ten un axente exclusivo en Nova Zelandia. Se estás interesado en mercar, a información de contacto é a seguinte:
Mick Dienhoff
Director xeral
Número de teléfono: 0755564763
Número de móbil: 0492 009 534
E-mail: enquiries@nzrapidtests.co.nz
Uso previsto
O casete de proba rápida de antíxeno SARSSTEP® SARS-CoV-2 emprega tecnoloxía de inmunocromatografía para detectar o antíxeno de nucleocápidos SARS-COV-2 no exemplar de tampón nasal anterior humano. Este único uso de testículos só está destinado a auto-proba. Recoméndase usar esta proba dentro dos 5 días despois do inicio dos síntomas. Está apoiado pola avaliación do rendemento clínico.
Introdución
A novela coronavirus pertence ao xénero Totiie P. Covid-19 é unha enfermidade infecciosa respiratoria aguda. A xente xeralmente é susceptible. Actualmente, os pacientes infectados pola novela cxjronavinis son a principal fonte de infección; As persoas infectadas asintomáticas tamén poden ser unha fonte infecciosa. Con base na investigación epidemiolóxica actual, o período de incubación é de 1 a 14 días, principalmente de 3 a 7 días. As principais manifestacións inclúen febre, fatiga e tose seca. A conxestión nasal, o nariz corrente, a dor de garganta, a mialxia e a diarrea atópanse en poucos casos.
Principio
A proba de antíxeno SARTSTEP® SARS-CoV-2 emprega unha proba inmunocromatográfica. Os anticorpos conxugados de látex (látex-AB) correspondentes ao SARS-CoV-2 están inmobilizados en seco ao final da franxa da membrana de nitrocelulosa. Os anticorpos SARS-CoV-2 son unidos na zona de proba (T) e a biotina-BSA é un enlace na zona de control (C). Cando se engade a mostra, migra por difusión capilar rehidratando o conxugado de látex. Se está presente na mostra, os antíxenos SARS-Cov-2 uniranse cos anticorpos conxugados que forman partículas. Estas partículas seguirán migrando ao longo da tira ata a zona de proba (T) onde son capturadas por anticorpos SARS-CoV-2 que xeran unha liña vermella visible. Se non hai antíxenos SARS-CoV-2 na mostra, non se forma ningunha liña vermella na zona de proba (T). O conxugado de estreptavidina seguirá migrando só ata que sexa capturado na zona de control (C) pola biotina-BSA que se agrega nunha liña azul, o que indica a validez da proba.
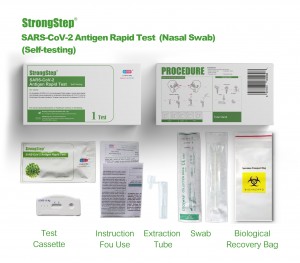
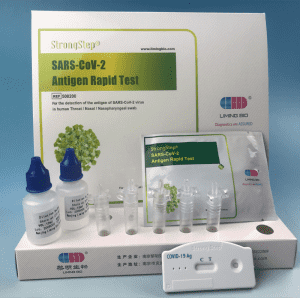
Compoñentes do kit
1 proba/caixa ; 5 probas/caixa :
| Dispositivos de proba envasados de bolsas de folla selado | Cada dispositivo contén unha tira con conxugados de cores e reactivos reactivos pre-espallados nas rexións correspondentes. |
| Frascos de tampón de dilución | 0,1 m de solución salina tamponada con fosfato (PBS) e 0,02% de azida de sodio. |
| Tubos de extracción | Para o uso de preparación de exemplares. |
| Paquetes de cotoneos | Para a recollida de exemplares. |
| Estación de traballo | Lugar para manter frascos e tubos tampón. |
| Inserir paquete | Para a instrución de operación. |
20 probas/caixa
| 20 dispositivos de proba envasados individualmente | Cada dispositivo contén unha tira con conxugados de cores e reactivos reactivos pre-repartidos nas reqions correspondentes. |
| 2 frascos de tampón de extracción | 0,1 m de solución salina tamponada con fosfato (P8S) e 0,02% azida de sodio. |
| 20 tubos de extracción | Para o uso de preparación de exemplares. |
| 1 estación de traballo | Lugar para manter frascos e tubos tampón. |
| 1 Inserir paquete | Para a instrución de operación. |
Materiais necesarios pero non proporcionados
| Temporizador | Para uso de cronometraxe. |
| Calquera equipo de protección persoal necesario |
PRECAUCIÓNS
-Este kit é só para uso diagnóstico in vitro.
- Lea atentamente as instrucións antes de realizar a proba.
- Este produto non contén materiais de fonte humana.
-Non use o contido do kit despois da data de caducidade.
Use luvas durante todo o procedemento.
Almacenamento e estabilidade
As bolsas seladas no kit de proba pódense almacenar entre 2-30 C durante a duración da vida útil como se indica na bolsa.
Recollida e almacenamento de exemplares
Pódese recoller unha mostra de tampón nasal anterior ou por un individuo Perfofmlng un auto-swab.
Os nenos menores de 18 anos deberían ser realizados pola súa supervisión de Aduk. Os adultos de 18 anos ou máis poden realizar por si mesmos o cotonete nasal anterior. Siga as súas directrices locais para a recollida de exemplares por parte dos nenos.
, Insira un hisopo nunha fosa nasal do paciente. A punta do hisopo debe inserirse ata 2,5 cm (1 polgada) desde o bordo da fosa nasal. Enrole o hisopo 5 veces ao longo da mucosa dentro da fosa nasal para asegurarse de que se recollan tanto o moco como as células.
• Use o mesmo hisopo, repita este proceso para outra fosa nasal para asegurarse de que se recolla unha mostra adecuada de ambas as cavidades nasais.
Recoméndase que os exemplares sexanprocesadoo antes posible despois da colección. Os exemplares pódense manter en hora de uptol de contedores a temperatura de mamá (15 ° C a 30 "c) ou ata 24 horas cando RSFrigeratod (2 ° C a 8eC) Antes do procesamento.
Procedemento
Traia dispositivos de proba, exemplares, tampón e/ou controis a temperatura ambiente (15-30 ° C).
♦PLAC® O tubo de extracción de exemplares recollidos na área designada da estación de traballo.
♦Presione todo o tampón de dilución no tubo de radión ext.
♦Coloque o cotonete no tubo. Mestura vigorosamente a solución xirando o hisopo contra o lado do tubo durante menos 15 veces (mentres está mergullado). Os mellores resultados obtéñense cando o exemplar se mestura vigorosamente na solución.
♦Permite que o hisopo se empape no tampón de extracción durante un minuto antes do seguinte paso.
♦Sacar o máximo de líquido posible do cotoneador pinchando o lado do tubo de extracción flexible a medida que se elimina o hisopo. Polo menos 1/2oftTie A solución de búfer de mostra debe permanecer no tubo para que se produza unha migración capilar adecuada. Poña a tapa no tubo extraído.
♦Descarta o hisopo nun recipiente de residuos biohazardos adecuado.
♦Os exemplares extraídos poden conservar a temperatura ambiente durante 30 minutos sen afectar o resultado da proba.
♦Elimina o dispositivo de proba THS da súa bolsa selada e colócaa nun decano e superficie a nivel. Etiqueta o dispositivo con paciente ou identificación de control. Para obter un mellor resultado, o ensaio debe realizarse dentro de 30 minutos.
♦Engade 3 gotas (aproximadamente 100 PL) de mostra extraída do tubo de extracción á mostra redonda ben no dispositivo de proba.
Evite atrapar burbullas de aire no pozo (s) da mostra e non solte ningunha solución na xanela de observación. A medida que a proba comeza a funcionar, verás que a cor se move pola membrana.
♦Verruga para que apareza a banda (s) de cores. O resultado debe ser lido por visual a 15 minutas. Non interprete o resultado despois de 30 minutos.
•Coloque o tubo de ensaio que contén o hisopo e o dispositivo de proba usado na bolsa biohazarda de cinta e selala, e logo descartalo nun recipiente de residuos adecuado. Logo tira os elementos restantes
•Lavadoas túas mans ou volven aplicar o desinfectante de mans.
Descarta os tubos de extracción usados e os dispositivos de proba en recipiente de residuos biohazardos adecuados.
V2.0_00.png)
Limitacións da proba
1- O kit está destinado a usar para a detección cualitativa OfSARS-Cov-2 antíxenos da nasal.
2. Esta proba detecta tanto viable) e SARS-Cov-2 viables e non viables. O rendemento da proba depende da cantidade de virus (antíxeno) na mostra e pode correlacionarse ou non cos resultados do cultivo viral perfonados na mesma mostra.
3. Pode producirse un resultado de teta negativa se o nivel de antíxeno nunha mostra está por debaixo do límite de detección da proba ou se a mostra foi recollida ou transportada de forma inadecuada.
4.Foilure para seguir o procedemento de proba pode afectar negativamente o rendemento da proba e/ou invalidar o resultado da proba.
5. Os resultados das probas deben correlacionarse coa historia clínica, os datos epidemiolóxicos e outros datos dispoñibles para o médico que avalía o paciente.
6. Os resultados das probas positivas non descartan co-infeccións con outros patóxenos.
7. Os resultados das probas negativas non están destinados a gobernar noutras infeccións virais ou bacterianas non SARS.
8. Os resultados negativos de pacientes con aparición de síntomas máis alá dos sete días, deben ser tratados como presuntos e confirmados cun ensaio molecular autorizado da FDA local, se é necesario, para a xestión clínica, incluído o control de infección.
9. As recomendacións de estabilidade de especie baséanse en datos de estabilidade das probas de gripe e o rendemento poden ser diferentes con SARS-Cov-2. Os usuarios deben probar exemplares o máis rápido posible despois da recollida de exemplares.
10. A sensibilidade para o ensaio RT-PCR no diagnóstico de CovID-19 é de só un 50% -80% debido á mala calidade da mostra ou ao punto de tempo da enfermidade na fase recuperada, etc.Sars-Cov-2 Antíxeno Rápido Device Device Device é teoricamente Baixa pola súa metodoloxía.
11. Por orde para obter o virus suficiente, suxírese usar dous ou máis tampóns para recoller diferentes sitios de mostra e extraer todo o tampón no mesmo tubo.
12. Os valores preditivos positivos e negativos dependen altamente das taxas de prevalencia.
13. Os resultados das probas positivas son máis propensos a representar resultados falsos positivos durante períodos de Little I Non SARS- COV-2 Actividade cando a prevalencia da enfermidade é baixa. alto.
14. Os anticorpos monoclonais poden non detectar ou detectar con menos sensibilidade, os virus da gripe SARS-Cov-2 que sufriron pequenos cambios de aminoácidos na rexión do epítopo diana.
15. O rendemento desta proba non se avaliou para o seu uso en pacientes sen signos e síntomas de infección respiratoria e parformidade pode diferir en individuos asintomáticos.
16. A cantidade de antíxeno nunha mostra pode diminuír a medida que aumenta a duración da enfermidade. Os exemplares recollidos despois do día 5 da enfermidade son máis propensos a ser negativos en comparación cun ensaio RT-PCR.
17. A sensibilidade da proba despois dos primeiros cinco días de aparición de síntomas demostrouse que diminúe en comparación cun ensaio RT-PCR.
18. É suxerido que use StrongStep® SARS-CoV-2 IgM/IgG Anticory Test Rapid (CAW 502090) para detectar o anticorpo para aumentar a sensibilidade do diagnóstico de CovID-19.
19. Non se recomenda empregar o exemplar de Medla (VTM) de Virus Transportation MedLA nesta proba, se os clientes insisten en usar este tipo de mostra, os clientes deberían validarse.
20. A proba rápida do antíxeno SARSSTEP® SARS-Cov-2 validouse cos tampóns fornecidos no kit. O uso de tampóns alternativos pode producir resultados falsos.
21. As probas frecuentes son necesarias para aumentar a sensibilidade do diagnóstico de COVID-19.
22. Non cae en sensibilidade en comparación co tipo salvaxe con raspado ás seguintes variantes - Voc1 Kent, Reino Unido, B.1.1.7 e Voc2 Sudáfrica, B.1.351.
23 Mantéñase fóra do alcance dos nenos.
24. Os resultados positivos indican que se detectaron antíxenos virais na mostra tomada, por favor auto-quinentena e informa pronto ao seu médico de familia.
1V2.0_01_副本.jpg)
Nanjing Liming Bio-Products Co., Ltd.
Nº 12 Huayuan Road, Nanjing, Jiangsu, 210042 PR China.
Tel: +86 (25) 85288506
Fax: (0086) 25 85476387
Correo electrónico:sales@limingbio.com
Sitio web: www.limingbio.com
Technical support: poct_tech@limingbio.com
Envases de produtos
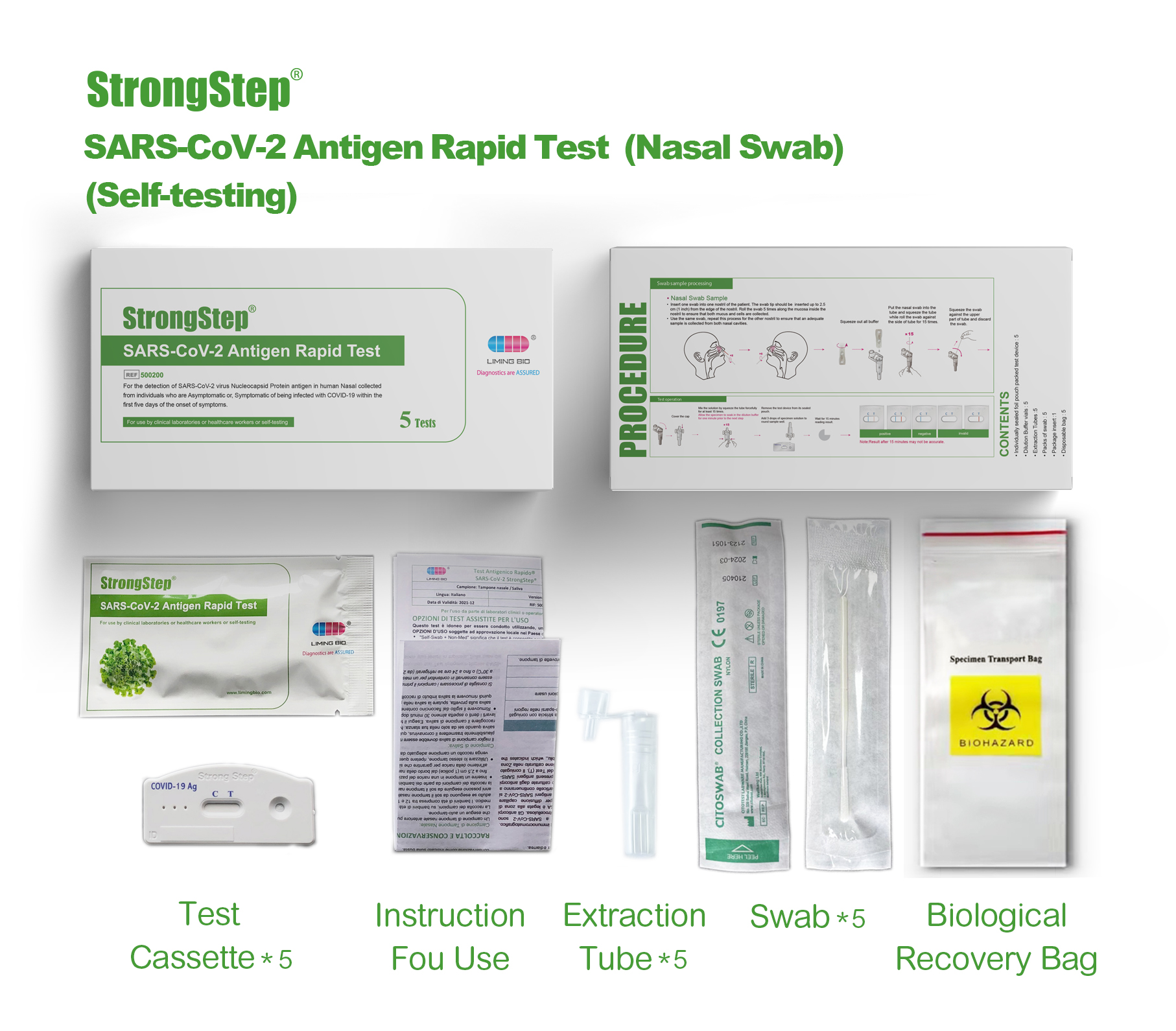
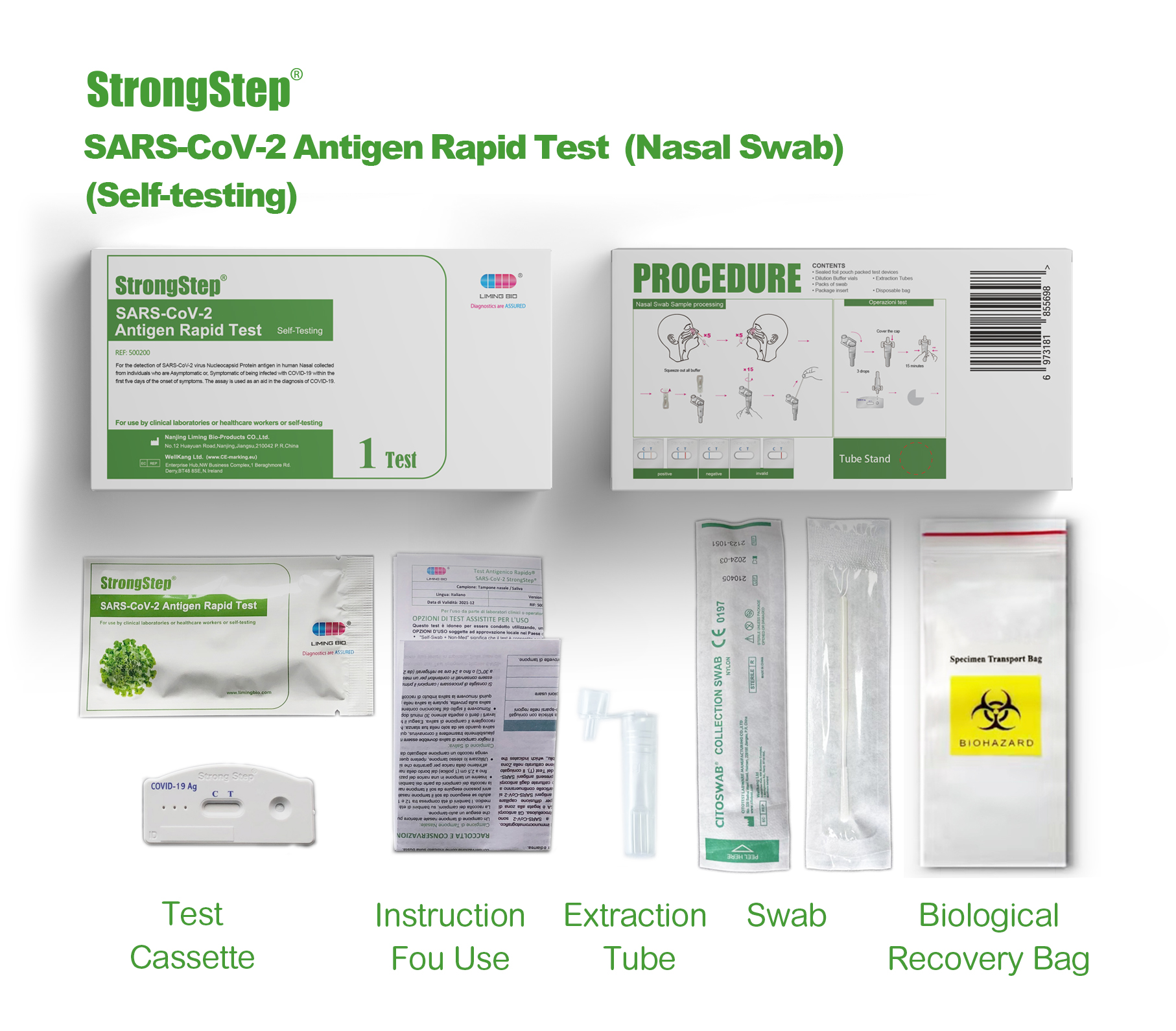






V2.01_00_副本.jpg)
1人份抗原卡实物图唾液版1_00_副本-300x216.png)