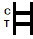Proba rápida de baile
Uso previsto
O forte®A proba de baile é unha proba inmunocromatográfica cualitativa e cualitativa para a detección de IGFBP-1 a partir de fluído amniótico en secrecións vaxinais durante o embarazo. A proba está destinada ao uso profesional para axudar a diagnosticar a rotura das membranas fetales (ROM) en mulleres embarazadas.
Introdución
A concentración de IGFBP-1 (proteína de unión do factor de crecemento como a insulina no fluído amniótico é de 100 a 1000 veces superior á do soro materno. O IGFBP-1 non está normalmente presente na vaxina, senón despois da ruptura das membranas fetales, o fluído amniótico cunha alta concentración de mesturas IGFBP-1 con secrecións vaxinais. Na proba de Prom StrongStep®, tómase un exemplar de secreción vaxinal cun hisopo de poliéster estéril e o exemplar é extraído en solución de extracción de exemplares. A presenza de IGFBP-1 na solución detéctase mediante un dispositivo de proba rápido.
Principio
O forte®A proba de promoción usa a tecnoloxía inmunocromatográfica de cor e tecnoloxía de fluxo capilar. O procedemento de proba require a solubilización de IGFBP-1 a partir dun hisopo vaxinal mesturando o hisopo en tampón de mostra. A continuación, o tampón de mostra mixto engádese á mostra de casete de proba ben e a mestura migra ao longo da superficie da membrana. Se IGFBP-1 está presente na mostra, formará un complexo co anticorpo anti-IGFBP-1 primario conxugado a partículas de cores. O complexo estará atado por un segundo anticorpo anti-IGFBP-1 recuberto na membrana de nitrocelulosa. A aparición dunha liña de proba visible xunto coa liña de control indicará un resultado positivo.
Compoñentes do kit
| 20 Individualmente pAckDispositivos de proba ed | Cada dispositivo contén unha tira con conxugados de cores e reactivos reactivos pre-recubertos nas rexións correspondentes. |
| 2ExtracciónVial de tampón | 0,1 m de solución salina tamponada con fosfato (PBS) e 0,02% de azida de sodio. |
| 1 hisopo de control positivo (só por petición) | Conteñen IGFBP-1 e azida de sodio. Para control externo. |
| 1 hisopo de control negativo (só por petición) | Non contén IGFBP-1. Para control externo. |
| 20 Tubos de extracción | Para o uso de preparación de exemplares. |
| 1 Estación de traballo | Lugar para manter frascos e tubos tampón. |
| 1 Inserir paquete | Para a instrución de operación. |
Materiais necesarios pero non proporcionados
| Temporizador | Para uso de cronometraxe. |
PRECAUCIÓNS
■ Para un uso diagnóstico profesional in vitro só.
■ Non use despois da data de caducidade indicada no paquete. Non use a proba se a súa bolsa de papel está danada. Non reutilizar as probas.
■ Este kit contén produtos de orixe animal. O coñecemento certificado da orixe e/ou estado sanitario dos animais non garante totalmente a ausencia de axentes patóxenos transmisibles. Por iso, recoméndase que estes produtos sexan tratados como potencialmente infecciosos e manexen observar as precaucións de seguridade habituais (non inxerir nin inhalar).
■ Evite a contaminación cruzada de exemplares mediante un novo recipiente de recollida de exemplares para cada exemplar obtido.
■ Lea con coidado todo o procedemento antes de realizar calquera proba.
■ Non come, beba nin fume na zona onde se manexan os exemplares e kits. Manexa todos os exemplares coma se conteñan axentes infecciosos. Observa as precaucións establecidas contra os riscos microbiolóxicos durante todo o procedemento e siga os procedementos estándar para a adecuada eliminación de exemplares. Use roupa de protección como abrigo de laboratorio, luvas desbotables e protección dos ollos cando se analizan os exemplares.
■ Non intercambia nin mestura reactivos de lotes diferentes. Non mestura tapóns de botellas de solución.
■ A humidade e a temperatura poden afectar negativamente os resultados.
■ Cando se complete o procedemento de ensaio, elimina os cotoniños con coidado despois de autoclavalos a 121 ° C durante polo menos 20 minutos. Alternativamente, pódense tratar con hipocloruro de sodio 0,5% (ou lixivia de casa) durante unha hora antes da eliminación. Os materiais de proba usados deben descartarse de acordo coas normativas locais, estatais e/ou federais.
■ Non use cepillos de citoloxía con pacientes embarazados.
Almacenamento e estabilidade
■ O kit debe almacenarse a 2-30 ° C ata a data de caducidade impresa na bolsa selada.
■ A proba debe permanecer na bolsa selada ata o seu uso.
■ Non conxelar.
■ Deberíase tomar coidados para protexer os compoñentes deste kit contra a contaminación. Non use se hai evidencias de contaminación ou precipitación microbiana. A contaminación biolóxica de equipos de dispensación, contedores ou reactivos pode levar a resultados falsos.
Recollida e almacenamento de exemplares
Use só dacron ou rayon inclinados tapóns estériles con eixes de plástico. Recoméndase empregar o hisopo subministrado polo fabricante de kits (os cotonetes non están contidos neste kit, para a información de pedido, póñase en contacto co fabricante ou distribuidor local, o número de cataloge é 207000). Non se validaron os cotonetes doutros provedores. Non se recomenda tampóns con puntas de algodón ou eixes de madeira.
■ Obtense unha mostra usando un hisopo de poliéster estéril. A mostra debe recollerse antes de realizar un exame dixital e/ou ecografía transvaginal. Teña coidado de non tocar nada co hisopo antes de tomar a mostra. Insira coidadosamente a punta do hisopo cara á vaxina cara á fornix posterior ata que se atope a resistencia. Alternativamente, a mostra pódese tomar da fornix posterior durante un exame de especulum estéril. O tampón debe deixarse na vaxina durante 10-15 segundos para permitirlle absorber a secreción vaxinal. Tire o cotonía con coidado!.
■ Poña o hisopo ao tubo de extracción, se a proba pode ser executada inmediatamente. Se non é posible probas inmediatas, as mostras do paciente deben colocarse nun tubo de transporte seco para o seu almacenamento ou transporte. Os cotonetes pódense almacenar durante 24 horas a temperatura ambiente (15-30 ° C) ou 1 semana a 4 ° C ou non máis de 6 meses a -20 ° C. Todos os exemplares deberían permitirse alcanzar unha temperatura ambiente de 15-30 ° C antes da proba.
Procedemento
Traia probas, exemplares, tampón e/ou controis a temperatura ambiente (15-30 ° C) antes do uso.
■ Coloque un tubo de extracción limpo na área designada da estación de traballo. Engade 1 ml de tampón de extracción ao tubo de extracción.
■ Poña o tampón no tubo. Mestura vigorosamente a solución xirando o hisopo contra o lado do tubo durante menos dez veces (mentres está mergullado). Os mellores resultados obtéñense cando o exemplar se mestura vigorosamente na solución.
■ Sacar o máximo de líquido posible do cotonía pinchando o lado do tubo de extracción flexible a medida que se elimina o hisopo. Polo menos 1/2 da solución de tampón de mostra debe permanecer no tubo para que se produza unha migración capilar adecuada. Poña a tapa no tubo extraído.
Descarta o hisopo nun recipiente de residuos biohazardos adecuado.
■ Os exemplares extraídos poden conservar a temperatura ambiente durante 60 minutos sen afectar o resultado da proba.
■ Retire a proba da súa bolsa selada e colócaa nunha superficie limpa e nivelada. Etiqueta o dispositivo con paciente ou identificación de control. Para obter un mellor resultado, o ensaio debe realizarse dentro dunha hora.
■ Engade 3 gotas (aproximadamente 100 µl) de mostra extraída do tubo de extracción ao pozo da mostra no casete da proba.
Evite atrapar burbullas de aire no pozo (s) do exemplar e non solte ningunha solución na xanela de observación.
A medida que a proba comeza a funcionar, verás que a cor se move pola membrana.
■ Agarde a que apareza a banda (s) de cores. O resultado debe lerse aos 5 minutos. Non interprete o resultado despois de 5 minutos.
Descarta os tubos de proba usados e os casetes de proba en recipiente de residuos biohazardos adecuados.
Nterpretación de resultados
| PositivoResultado:
| Na membrana aparecen dúas bandas de cores. Unha banda aparece na rexión de control (C) e outra banda aparece na rexión de proba (T). |
| NegativoResultado:
| Só aparece unha banda de cores na rexión de control (C). Non aparece ningunha banda aparente de cor na rexión de proba (T). |
| Non válidoResultado:
| A banda de control non aparece. Debe descartarse os resultados de calquera proba que non produciu unha banda de control no tempo de lectura especificado. Revisa o procedemento e repita cunha nova proba. Se o problema persiste, descontinúa usando o kit inmediatamente e póñase en contacto co seu distribuidor local. |
Nota:
1. A intensidade da cor na rexión de proba (T) pode variar segundo a concentración de substancias dirixidas presentes no exemplar. Pero o nivel de substancias non se pode determinar por esta proba cualitativa.
2. O volume de exemplar insuficiente, o procedemento de operación incorrecto ou a realización de probas caducadas son as razóns máis probables para o fallo da banda de control.
Control de calidade
■ Na proba están incluídos os controis procesuais internos. Unha banda de cores que aparece na rexión de control (C) considérase un control procesual positivo interno. Confirma o volume suficiente de exemplares e a técnica de procedemento correcta.
■ Os controis procedementais externos poden proporcionar (só a solicitude) nos kits para asegurarse de que as probas funcionen correctamente. Ademais, os controis poden usarse para demostrar un rendemento adecuado polo operador de proba. Para realizar unha proba de control positiva ou negativa, complete os pasos na sección de procedemento de proba tratando o tampón de control do mesmo xeito que un tampón de exemplar.
Limitacións da proba
1. Non se debe facer unha interpretación cuantitativa en función dos resultados da proba.
2. Non use a proba se a súa bolsa de papel de aluminio ou os selos da bolsa non están intactos.
3. Un forte positivo®Resultado da proba de baile, aínda que detectar a presenza de líquido amniótico na mostra, non localiza o sitio da ruptura.
4.As con todas as probas de diagnóstico, os resultados deben interpretarse á luz doutros achados clínicos.
5. Se se produciu a ruptura das membranas fetales, pero a fuga de líquido amniótico cesou máis de 12 horas antes de que se tomase o exemplar, IGFBP-1 pode ser degradado por proteasas na vaxina e a proba pode dar un resultado negativo.
Características de rendemento
Táboa: StrongStep®Proba de baile fronte a outra proba de baile de marca
|
Sensibilidade relativa: |
| Outra marca |
| ||
| + | - | Total | |||
| Strongstep®Prom Proba | + | 63 | 3 | 66 | |
| - | 2 | 138 | 140 | ||
|
| 65 | 141 | 206 | ||
Sensibilidade analítica
A menor cantidade detectable de IGFBP-1 na mostra extraída é de 12,5 μg/L.
Substancias interferindo
Hai que ter coidado de non contaminar a aplicadora ou secrecións cervicovaginais con lubricantes, xabóns, desinfectantes ou cremas. Os lubricantes ou as cremas poden interferir físicamente coa absorción do exemplar no aplicador. Os xabóns ou desinfectantes poden interferir na reacción de anticorpos-antíxeno.
As substancias interferidas potenciais probáronse a concentracións que se poderían atopar razoablemente nas secrecións cervicovaginais. As seguintes substancias non interferiron no ensaio cando se probaron nos niveis indicados.
| Sustancia | Concentración | Sustancia | Concentración |
| Ampicilina | 1,47 mg/ml | Prostaglandina F2 | 0,033 mg/ml |
| Eritromicina | 0,272 mg/ml | Prostaglandin E2 | 0,033 mg/ml |
| 3º trimestre de orina materna | 5% (vol) | Monistatr (miconazol) | 0,5 mg/ml |
| Oxitocina | 10 UI/ml | Indigo Carmine | 0,232 mg/ml |
| Terbutalina | 3,59 mg/ml | Gentamicina | 0,849 mg/ml |
| Dexametasona | 2,50 mg/ml | Xel de Betadiner | 10 mg/ml |
| MGSO4•7h2o | 1,49 mg/ml | Limpador de Betadiner | 10 mg/ml |
| Ritodrina | 0,33 mg/ml | Marmelada K-yr | 62,5 mg/ml |
| Dermicidolr 2000 | 25,73 mg/ml |
Referencias da literatura
Erdemoglu e Mungan T. Significación de detectar a proteína-1 de unión do factor de crecemento como a insulina en secrecións cervicovaginais: comparación coa proba de nitrazina e avaliación do volume de fluído amniótico. Acta Obstet Gynecol Scand (2004) 83: 622-626.
Kubota T e Takeuchi H. Avaliación da proteína de unión do factor de crecemento como a insulina como ferramenta de diagnóstico para a ruptura das membranas. J Obstet Gynecol Res (1998) 24: 411-417.
Rutanen Em et al. Avaliación dunha proba rápida de tira para a proteína-1 de unión do factor de crecemento como a insulina no diagnóstico de membranas fetales roturadas. Clin Chim Acta (1996) 253: 91-101.
Rutanen EM, Pekonen F, Karkkainen T. Medición da proteína-1 de unión do factor de crecemento como a insulina en secrecións cervicais/vaxinais: comparación coa inmunoensay de membrana rom-comproba no diagnóstico de membranas fetales roturadas. Clin Chim Acta (1993) 214: 73-81.
Glosario de símbolos
|
| Número de catálogo |  | Limitación da temperatura |
 | Consulte as instrucións para o seu uso |
| Código por lotes |
 | Dispositivo médico de diagnóstico in vitro |  | Usar por |
 | Fabricante |  | Contén suficiente para |
 | Non reutilizar |  | Representante autorizado na Comunidade Europea |
 | CE marcado segundo a Directiva de Dispositivos Médicos IVD 98/79/CE | ||